Química Orgánica I-B, Semestre B-09
Tarea 1
1) Para las siguientes moléculas, dibuje estructuras tipo Lewis y tridimensionales y indique el tipo de hibridación de los átomos de Boro, Carbono, y Nitrógeno; los momentos dipolares de los enlaces, y el momento dipolar de la molécula entera. Use líneas punteadas y cuñas en el caso de una estructura tridimensional.
a) BF3, b) HCl, c) CH2Cl2, d) CCl4, e) CHCl3, f)Cl2NH,
g) H2C=CCl2, h) H2C=C=NNH2.
2) Compare dos modelos de estructura molecular aplicados a NF3 y de NH3. El primero de estos modelos es con los orbitales atómicos del Nitrógeno central con hibridación sp3 y el segundo es con los orbitales no-hibridizados. Determine (cualitativamente) el momento dipolar de cada molécula para cada caso. Compare su resultado con él determinado experimentalmente: NH3, μ=1.46D; y NF3, μ=0.24D
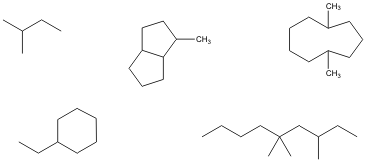
3) Identifique todos los átomos de carbono en las siguientes estructuras como 1°, 2°, 3°, o 4°, según sea el caso.

4) Para las siguientes moléculas, dibuje representaciones de las maneras en que se pueden formar puentes hidrógenos (entre todas las moléculas presentes) tanto en la sustancia pura como en solución acuosa.
a) HF, b) N(CH3)3, c) CH2F2, d) CH3OH. e) HN(CH3)2