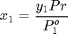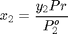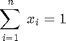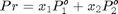Contents
Equilibrio líquido-vapor de sistemas ideales
Se tiene una mezcla equimolar de 1-propanol y 2-propanol a la Temperatura de 60^oC. Calcule:
- Presión de rocío de la solución
- Presión de burbuja de la solución
- La proporción de Vapor y Líquido, y sus respectivas composiciones ... cuando la mezcla se somete a una presión igual al promedio aritmético entre la Presión de Burbuja y la Presión de Rocío.
La presión de vapor de los componentes puros puede calcularse mediante la ecuación de Antoine:
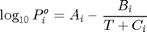
P en mmHg y T en ^oC
disp ('Compuesto A B C') disp('1- Propanol 8,37895 1788,02 227,438') disp('2- Propanol 8,87829 2010,32 252,636') %
Compuesto A B C 1- Propanol 8,37895 1788,02 227,438 2- Propanol 8,87829 2010,32 252,636
Preparación e introducción de datos
clear all % Borramos toda posible variable clc % Limpiamos la pantalla de comando close all % Cerramos toda ventana de figura % Debemos chequear que el iso-propanol es más volátil que el 1-propanol % Definimos que: (1):2-propanol (2):1-propanol A=[8.87829 8.37895 ]; B=[2010.32 1788.02 ]; C=[252.636 227.438 ]; z=[0.5 1-0.5]; % Composición de la solución original T= 60; % Temperatura del sistema (constante)
Modelo descriptivo para el ELV
El sistema 1-propanol/2-propanol se comporta a la temperatura de 60^oC puede modelarse usando la ecuación de gas ideal para la fase vapor (presiones de vapor de los compuestos muy por debajo de la presión crítica), y la ecuación de Raoult para la fase líquida (sustancias muy similares en forma, tamaño y polaridad; cuya presión de vapor está cercana a la presión total del sistema).
Presión de burbuja (Pb)
A temperatura constante, la presión de vapor de los compuestos puros permanece constante. La calculamos usando la ecuación de Antoine
P1vap=10.^(A(1)-B(1)./(T+C(1))); % mmHg P2vap=10.^(A(2)-B(2)./(T+C(2))); % mmHg
En el punto de burbuja la composición del líquido no difiere de aquella de la solución original
x=z; Pb=x(1)*P1vap+x(2)*P2vap yb=x(1)*P1vap/Pb
Pb =
2.123001271754318e+02
yb =
0.660821530054008
La presión de burbuja es de 212.3 mmHg y la primera burbuja de vapor por expansión isotérmica tiene una composición molar de en 1-propanol de 66.1% (máxima posible para el vapor proveniente de la destilación de la solución original)
Presión de rocío (Pr)
En el punto de rocío, la composición del vapor no difiere de aquella de la solución original, y la composición del líquido es desconocida
y=z;
Uniendo las ecuaciones 1 y 2 debe cumplirse que:
Si mezclamos ambas ecuaciones, tendremos una ecuación con una sola incógnita, x_1, que nos permitirá definir la función a resolver
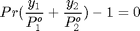
f=@(x1) (x1*P1vap+(1-x1)*P2vap)*(y(1)/P1vap+y(2)/P2vap)-1; xrocio=fsolve(f,0.2) Pr=xrocio*P1vap+(1-xrocio)*P2vap
Equation solved.
fsolve completed because the vector of function values is near zero
as measured by the default value of the function tolerance, and
the problem appears regular as measured by the gradient.
xrocio =
0.339178470112729
Pr =
1.903367750434110e+02
La presión de rocio es 190.34 mmHg y la última gota de líquido (durante expansión isotérmica) tiene una composición de 33.92% de 2-propanol, o sea 66.08 % molar en 1-propanol (máxima posible para el líquido proveniente de la destilación de la solución original)
Destilación Flash a T=60^oC y P=(Pb+Pr)/2
P=mean([Pb Pr]) % Presión promedio entre la de burbuja y rocío
P =
2.013184511094214e+02
En este caso deben satisfacerse las ecuaciones del balance de masa y del equilibrio líquido-vapor:
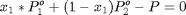 $
$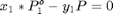

Se tienen tres ecuaciones con tres incógnitas: x_1, y_1, fvap Creamos un archivo auxiliar llamado ELVnPropisoPropanolf.m Este archivo DEBE ESTAR GUARDADO en la misma carpeta de trabajo donde se encuentre el archivo de este problema
Resolución del sistema de ecuaciones
Usamos la función fsolve de MatLab y usamos un vector de condiciones iniciales. Debemos crear variables globales para facilitar la resolución
global z global P global P1vap global P2vap soluciones=fsolve(@ELVnPropisoPropanolf,[0.5 0.5 0.5])
Warning: The value of local
variables may have been
changed to match the
globals. Future
versions of MATLAB
will require that
you declare
a variable to be
global before you
use that variable.
Warning: The value of local
variables may have been
changed to match the
globals. Future
versions of MATLAB
will require that
you declare
a variable to be
global before you
use that variable.
Warning: The value of local
variables may have been
changed to match the
globals. Future
versions of MATLAB
will require that
you declare
a variable to be
global before you
use that variable.
Warning: The value of local
variables may have been
changed to match the
globals. Future
versions of MATLAB
will require that
you declare
a variable to be
global before you
use that variable.
Equation solved.
fsolve completed because the vector of function values is near zero
as measured by the default value of the function tolerance, and
the problem appears regular as measured by the gradient.
soluciones =
0.419589235056365 0.584797074312514 0.486724875191714
La destilación Flash de la solución equimolar a la presión de 201.3 mmHg y 60^oC permite obtener un líquido con una composición molar 41.95% y un vapor de composición molar 58.5% molar en 2-propanol, logrando un 48.7% de vaporización. Observamos que la separación no es eficiente, puesto que los compuestos tienen volatilidades similares. La volatilidad relativa a 60 ^oC es sólo de 1.95 (\alpha)