


Next: Cálculo estadístico de la
Up: Termodinámica
Previous: Cálculo cinético de la
Usando el resultado anterior y la ecuación de estado para un gas ideal,
se puede encontrar que
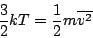 |
(13) |
o equivalentemente que
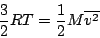 |
(14) |
A partir de este resultado obtenemos
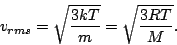 |
(15) |
Willians Barreto
2006-04-24